| Nombre completo oficial |
Factor de crecimiento epidérmico humano recombinante (rHuEGF) |
| secuencia |
 |
| Secuencia de aminoácidos |
NSDSECPLSH DGYCLHDGVC MYIEALDKYA CNCVVGYIGE RCQYRDLKWW ELR |
| Sinónimos |
Urogastrona, URG |
| Número de acceso |
P01133 |
| ID de gen |
|
| Resumen |
El factor de crecimiento epidérmico (EGF) se descubrió originalmente en preparaciones crudas de factor de crecimiento nervioso preparado a partir de las glándulas submaxilares de ratón como una actividad que inducía la apertura temprana del párpado, la erupción de los incisivos, la inhibición del crecimiento del cabello y el retraso en el crecimiento cuando se inyectaba en ratones recién nacidos. El EGF humano se aisló de la orina en función de su efecto inhibidor sobre la secreción gástrica y, en consecuencia, se denominó urogastrona. El EGF es un prototipo de una familia de factores de crecimiento que se derivan de precursores anclados a la membrana. Todos los miembros de esta familia se caracterizan por la presencia de al menos una unidad estructural EGF (definida por la presencia de un motivo de 6 cisteínas conservado que forma tres enlaces disulfuro) en su dominio extracelular. El EGF se sintetiza inicialmente como una proteína transmembrana precursora de 130 kDa que contiene 9 unidades de EGF. La secuencia de EGF soluble madura corresponde a la unidad de EGF ubicada próxima al dominio transmembrana. El precursor de EGF de membrana es capaz de unirse al receptor de EGF y se informó que es biológicamente activo. El EGF humano maduro comparte 70% de identidad de secuencia de aa con EGF de ratón y rata maduros. |
| Fuente |
Escherichia coli. |
| Peso molecular |
Aproximadamente 6.2 kDa, una única cadena polipeptídica no glicosilada que contiene 53 aminoácidos. |
| Actividad biológica |
Totalmente biológicamente activo en comparación con el estándar. La DE50 determinada por un ensayo de proliferación celular usando células Balb / c 3T3 murinas es menor de 1 ng / ml, correspondiente a una actividad específica de> 1.0 x 106 UI / mg. |
| Apariencia |
Polvo blanco liofilizado (liofilizado) filtrado estéril. |
| Formulación |
Liofilizado a partir de una solución concentrada filtrada de 0.2 um en PBS, pH 7.4. |
| endotoxina |
Menos de 1 UE / ug de rHuEGF según lo determinado por el método LAL. |
| Reconstitución |
Recomendamos que este vial se centrifugue brevemente antes de abrirlo para llevar el contenido al fondo. Reconstituya en agua destilada estéril o tampón acuoso que contenga 0.1% de BSA a una concentración de 0.1-1.0 mg / mL. Las soluciones madre deben distribuirse en alícuotas de trabajo y almacenarse a ≤ -20 ° C. Deben realizarse diluciones adicionales en soluciones tamponadas adecuadas. |
| Estabilidad y almacenamiento |
Utilice un congelador de descongelación manual y evite ciclos repetidos de congelación-descongelación.- 12 meses desde la fecha de recepción, -20 a -70 ° C como se suministra.- 1 mes, 2 a 8 ° C en condiciones estériles después de la reconstitución.- 3 meses, -20 a -70 ° C en condiciones estériles después de la reconstitución. |
| Referencias |
|
| SDS-PAGE |
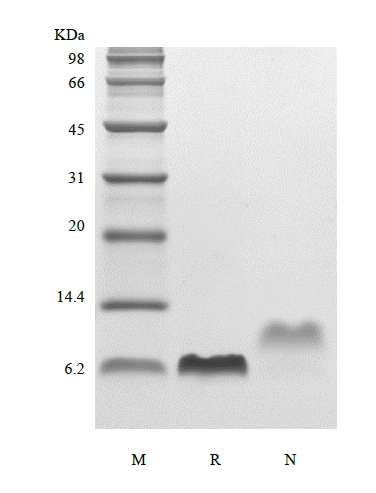 |
| Descarga de la hoja de datos de seguridad (SDS) |
Haz clic para descargar |
| Descarga de la hoja de datos técnicos (TDS) |
Haz clic para descargar |



